Show
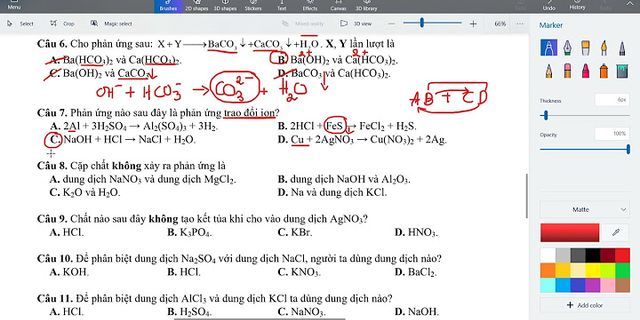
BaCl2 + K2SO4 → 2KCl + BaSO4↓ Quảng cáo Điều kiện phản ứng - Không có Cách thực hiện phản ứng - Cho BaCl2 phản ứng với dung dịch K2SO4 Hiện tượng nhận biết phản ứng - Xuất hiện kết tủa trắng bari sunfat trong dung dịch Bạn có biết CaCl2 cũng có phản ứng tương tự tạo kết tủa trắng CaSO4 Ví dụ 1: Chỉ dùng một thuốc thử phân biệt các kim loại sau: Mg, Zn, Fe, Ba? A. Nước. B. Dung dịch H2SO4 loãng. C. Dung dịch NaCl. D. Dung dịch NaOH. Đáp án: B Hướng dẫn giải Cho lần lượt các kim loại tác dụng với axit nếu thấy có kết tủa là Ba. Cho Ba vào các dung dịch muối còn lại nếu thấy: Có kết tủa sau đó kết tủa tan thì đó là: Zn Có kết tủa trắng hơi xanh là: Fe Có kết tủa trắng là: Mg Quảng cáo Ví dụ 2: Hiện tượng xảy ra khi sục từ từ khí CO2 đến dư vào dung dịch Ba(OH)2 là: A. Xuất hiện kết tủa trắng. B. Ban đầu tạo kết tủa trắng, sau đó tan dần. C. Sau 1 thời gian mới xuất hiện kết tủa trắng. D. Không xuất hiện kết tủa. Đáp án: B Hướng dẫn giải CO2 + Ba(OH)2 → BaCO3↓ + H2O (Lúc đầu OH- rất dư so với CO2) BaCO3 + CO2 + H2O → Ba(HCO3)2
Giới thiệu kênh Youtube VietJack



phuong-trinh-hoa-hoc-cua-bari-ba.jsp
Chủ đề Công cụ hóa học Phương trình hóa học Chất hóa học Chuỗi phản ứng
Phản ứng nhiệt phân Phản ứng phân huỷ Phản ứng trao đổi Lớp 11
Phản ứng oxi-hoá khử Lớp 10 Lớp 9 Phản ứng thế
Phản ứng hoá hợp Phản ứng nhiệt nhôm Lớp 8 Phương trình hóa học vô cơ
Phương trình thi Đại Học Phản ứng điện phân Lớp 12 Phản ứng thuận nghịch (cân bằng)
Phán ứng tách Phản ứng trung hoà Phản ứng toả nhiệt Phản ứng Halogen hoá
Phản ứng clo hoá Phản ứng thuận nghịch Phương trình hóa học hữu cơ Phản ứng đime hóa
Phản ứng cộng Phản ứng Cracking Phản ứng Este hóa Phản ứng tráng gương
Phản ứng oxi hóa - khử nội phân tử Phản ứng thủy phân Phản ứng Anxyl hoá Phản ứng iot hóa
Phản ứng ngưng tụ Phán ứng Hydro hoá Phản ứng trùng ngưng Phản ứng trùng hợp
Dãy điện hóa Dãy hoạt động của kim loại Bảng tính tan Bảng tuần hoàn
Tìm kiếm phương trình hóa học nhanh nhấtTìm kiếm phương trình hóa học đơn giản và nhanh nhất tại Cunghocvui. Học Hóa không còn là nỗi lo với Chuyên mục Phương trình hóa học của chúng tôi
Hướng dẫn
Bạn hãy nhập các chất được ngăn cách bằng dấu cách ' ' Một số ví dụ mẫu
Hướng dẫn
BaCl2 + H2SO4 - Cân bằng phương trình hóa học
Chi tiết phương trình
Thông tin thêm
Điều kiện: Không có Cách thực hiện: Cho vào ống nghiệm 1ml dung dịch H2SO4 loãng. Sau đó nhỏ vào ống nghiệm 3-4 giọt dung dịch BaCl2 Hiện tượng: Xuất hiện kết tủa trắng bari sunfat (BaSO4) trong dung dịch. Bạn có biết: Gốc sunfat (=SO4) trong phân tử H2SO4 kết hợp với nguyên tố bari trong phân tử BaCl2 tạo ra kết tủa trắng là bari sunfat. Muối có thể tác dụng được với axit, sản phẩm là muối mới và axit mới. Tính khối lượngLớp 9 Lớp 10 Phản ứng trao đổi Nếu thấy hay, hãy ủng hộ và chia sẻ nhé!
Phương trình điều chế BaCl2 Xem tất cả
Phương trình điều chế H2SO4 Xem tất cả
Phương trình điều chế HCl Xem tất cả
Phương trình điều chế BaSO4 Xem tất cả
Bài liên quan
|